
…siamo metodi o ufficiali?
Ogni tanto ci piace tornare a riscoprire certe perle del documento Accredia RT 08. La fonte di ispirazione pare inesauribile.
Oggi vediamo cosa si propone di interessante al punto 7.2 del documento, quello che riguarda selezione, verifica e validazione dei metodi.
Il punto 7.2 della ISO 17025 è in generale piuttosto chiaro, e il primo sottopunto, il 7.2.1.1, non fa eccezione:
“Il laboratorio deve utilizzare metodi e procedure appropriati per tutte le attività di laboratorio e, ove opportuno, per la valutazione dell’incertezza di misura, così come tecniche statistiche per l’analisi dei dati”
Ci pare tutto detto, è necessario aggiungere qualcosa ad “appropriati”? Qualcuno pensa di sì. Cominciamo bene: al punto 7.2.1.1 dell’RT 08 si “rammenta” (ci piace molto il linguaggio usato, a metà tra circolare ministeriale e avviso dell’amministratore nell’androne del condominio) che “i Laboratori preposti al controllo ufficiale (es. dei prodotti alimentari) sono tenuti a verificare che tutti i metodi di prova siano conformi a quanto stabilito nelle specifiche Direttive/Regolamenti in vigore” (le maiuscole messe a caso sono roba loro, come sempre, così come le barre al posto delle congiunzioni).
Ne possiamo dedurre che tutto ciò non vale per i laboratori non preposti al controllo ufficiale? Sarebbe alquanto strano. Visto che la norma prevede che i metodi siano “appropriati” in ogni caso.
Da notare poi il riferimento esclusivo a “Direttive-barra-Regolamenti”. E per quanto riguarda leggi, decreti, circolari (vincolanti per la pubblica amministrazione, quindi anche per i laboratori pubblici), nulla?
Le modifiche consentite
Sempre al punto 7.2.1.1 del documento RT 08 si discute di modifiche ai metodi.
Peccato che la norma ISO 17025 tratti la questione al punto 7.2.1.7, non al 7.2.1.1, ma è un dettaglio… Parecchi punti dell’RT 08 sono messi lì a casaccio. Non poteva mancare uno sfasamento rispetto alla norma nel punto più caotico del documento, assieme al 7.11.
La norma ISO 17025 consente scostamenti ai metodi solo se “documentati, tecnicamente giustificati, autorizzati e accettati dal cliente”.
Il documento RT 08 limita questa possibilità, consentendo le modifiche ai metodi solo in caso di miglioramento delle prestazioni (per migliorie che non alterino principio e tecnica). In questo caso, secondo RT 08, è consentito mantenere i riferimenti al metodo (“ufficiale/normalizzato/non normalizzato” scrivono loro), previa “verifica” delle prestazioni stesse.
Notiamo il riferimento a “metodo ufficiale”. Ne discuteremo a breve.
Nel caso di estensioni, sia del campo di misura che di quello di applicazione, la modifica è consentita ma è richiesta “validazione”. Negli altri casi la modifica non è consentita.
Da notare il richiamo a metodi che prevedono la possibilità di estensione applicativa “per ulteriori parametri non previsti”.
“Si ricorda che alcuni metodi indicano la possibilità di ampliarne l’impiego per la determinazione di ulteriori parametri non previsti; il Laboratorio può aggiungerli previa validazione degli stessi”
Questo richiamo ha tutta l’aria di essere stato inserito ad metodus (oltre ai provvedimenti ad personam e ad riservam esistono anche questi e l’RT 08 ne abbonda: di molti ricordiamo la storia e l’evoluzione dagli albori; come cantava il Poeta “prima cambiarono il giudice e subito dopo la legge”). Esso ci ricorda infatti molto bene una vecchia questione emersa agli albori della “DA online”, quando in via Saliceto decisero di “sistemare” gli elenchi dei metodi accreditati. Di colpo i laboratori che avevano accreditato gli zuccheri in HPLC secondo IstiSan 96/34, pag. 66, si sono visti cancellare dall’elenco metodi accreditati il parametro Lattosio. Questo perché il metodo, pur recando nel titolo “Carboidrati singoli o in miscela”, omette di indicare tra i reagenti lo standard per il Lattosio. Un po’ esagerato? A noi, che un po’ di gavetta in laboratorio l’abbiamo fatta, anche prima della nascita dell’accreditamento, pare di sì.
Ah, i metodi IstiSan 96/34 in Accredia sono proprio considerati male e trattati peggio. Ci ritorneremo fra un attimo.
Ma cosa sono i metodi “ufficiali”?
(e soprattutto, esistono?)
La risposta a questa domanda ce la vorrebbe fornire il documento RT 08, che riporta la seguente definizione:
“Metodo di prova ufficiale: Metodo di prova riportato o richiamato in documenti normativi cogenti e/o pubblicato su Gazzetta Ufficiale Italiana (GU) o dell’Unione Europea (GUCE) o comunque richiamato o riportato in un documento emesso da una Autorità Competente (es. Ministero, Regione, Provincia, ecc.)”.
Va notato innanzitutto però che la ISO 17025 non menziona affatto il termine “metodi ufficiali”, abbondantemente utilizzato nel documento RT 08. La norma cita “metodi pubblicati”, “metodi normalizzati”, “metodi non normalizzati”, “metodi sviluppati dal laboratorio”. Si tratta di un’aggiunta dei redattori del documento, foriera di confusione.
A cosa corrispondono i termini utilizzati nella norma? Vediamolo, poi torniamo ai metodi “ufficiali”.
Metodi pubblicati
Per i metodi pubblicati è ovvio e tautologico che si tratti di metodi in qualche modo “pubblicati”. Sarebbe meglio (raccomandato dalla norma) se a cura di “organizzazioni tecniche autorevoli” o in pubblicazioni “di rilevanza scientifica”. A nostro parere non si possono nemmeno escludere metodi pubblicati esclusivamente sul web.

Metodi normalizzati
I metodi normalizzati, per i quali nessun documento primario riporta una definizione, dovrebbero essere, secondo la lingua italiana, quelli contenuti in norme, sia di tipo volontario come quelle emesse da organismi normatori o da agenzie statali (ad esempio ISO 6579 per Salmonella in alimenti, EPA 7473 per Mercurio in acque – i metodi EPA sono da considerare cogenti in USA ma volontari in Italia), sia di tipo cogente (ad esempio Reg. CE 2568 del 1991 per Acidi grassi in olio d’oliva, D.M. 10 febbraio 2015 per Coliformi totali ed Escherichia coli in acque minerali).
Secondo l’RT 08 sono in effetti più o meno questi, ma con qualche ritocco che complica le cose:
“Metodo di prova normalizzato: metodo approvato da organismi di normazione nazionali, europei o internazionali (ad es. metodi UNI, CEI, CEN, ISO, UNICHIM, ASTM, AOAC, ecc.) o da organismi pubblici autorevoli (es. USDA, FDA, EPA, NIOSH, IUPAC, APHA, OIV, OIE, WHO, APAT, CNR, IRSA, ISPRA, NMKL, ecc.)”.
anche se in realtà né UniChim, né AOAC sono propriamente organismi di normazione: si tratta di associazioni non investite di alcun ruolo istituzionale come invece è ad esempio per l’UNI (vedere art. 1 dello Statuto UNI). Così come APHA, OIV, OIE, NMKL, WHO, non sono “organismi pubblici”, bensì associazioni o organizzazioni non governative.
Di fatto UniChim, AOAC, APHA, OIV, OIE, NMKL, WHO APHA, OIV, OIE, NMKL, WHO sono “organizzazioni tecniche nazionali o internazionali”.
Metodi non normalizzati
I metodi NON normalizzati sono ovviamente quelli diversi da quelli normalizzati. In linea di principio, secondo le indicazioni della norma, quelli pubblicati da organizzazioni o in libri, siti web, riviste scientifiche ma non riferibili a norme cogenti o volontarie. Sono senz’altro metodi che sono stati “pubblicati” ma non in norme. Per questi metodi la norma richiede validazione (punto 7.2.2.1).
Secondo RT 08 sono invece “metodi emessi da organizzazioni tecniche nazionali o internazionali, metodi sviluppati da Laboratori/centri di riferimento nazionali o comunitari o da centri di referenza nazionali accreditati”.
Notiamo che le “organizzazioni tecniche nazionali o internazionali” comprendono ad esempio proprio NMKL, WHO, OIV, AOAC, UniChim, ecc. Quindi occorrerebbe validarli? Pare di no, dovrebbe valere l’inclusione tra i metodi normalizzati presente tra gli esempi riportati nella definizione. La confusione aumenta.
L’RT 08 aggiunge poi, sempre nella definizione, che “Uno degli elementi discriminanti, rispetto ai metodi normalizzati, è che la responsabilità dei dati forniti è riferita non all’organizzazione che lo ha emesso, ma ai singoli autori”.
Il documento RT 08 raggiunge vette di confusione sempre maggiori al punto 7.2.2 richiedendo la validazione per questi metodi pur considerandoli normalizzati:
“I metodi normalizzati e i metodi ufficiali sono considerati validati dall’ente che li ha emessi, a meno che la responsabilità dei dati forniti sia riferita non all’organizzazione che li ha emessi, ma ai singoli autori”
Quindi, proviamo a ricapitolare il pensiero dei redattori dell’RT 08:
- I “metodi emessi da organizzazioni tecniche nazionali o internazionali” sono NON normalizzati ma per essi la validazione non è necessaria;
- I metodi normalizzati (o ufficiali) con dati forniti dagli autori, di cui essi sono responsabili, richiedono validazione.

Arzigogolato assai. E completamente opposto a quanto chiaramente espone la norma!
Perché tutto questo?
Come è noto l’eccezione è riferita ai metodi IstiSan per alimenti contenuti nel rapporto 96/34 e nel rapporto 96/35 e trae inizialmente spunto dalla frase riportata nell’introduzione alla raccolta “in alcuni casi si reputa necessario attendere il responso derivante dall’impiego in circuiti di validazione”, dal fatto che i metodi della raccolta non riportano dati di validazione e dalla presenza del riferimento agli autori dei metodi nel testo, in corrispondenza di ciascun metodo chimico. Ciò non volendo considerare che, come riportato nella stessa introduzione, “la gran parte delle metodiche sia stata ampiamente sperimentata e quindi da ritenersi di provata affidabilità” e che moltissimi metodi normalizzati, anche ISO e “ufficiali”, non riportano a loro volta alcun dato di validazione. Anche la maggior parte dei metodi Unichim non riporta alcun dato di validazione. Ma in questo caso nessun problema. Per i metodi ISS invece ringraziamo lo zelo di qualche ispettore, all’epoca desideroso di mettersi in mostra…
Insomma, è abbastanza evidente che i metodi IstiSan sugli alimenti stanno sugli zebedei a qualcuno ma si è voluto evitare di scrivere in RT 08 “i metodi Istisan sugli alimenti ve li vogliamo far validare a ogni costo”.
CNR, ISPRA, IRSA sì ma ISS no. Ciccia!

Raccolte successive ISS (esempio rapporto 07/31) non riportano le frasi nell’introduzione né i nomi degli autori e quindi i metodi ivi contenuti sono considerati già validati, anche se non riportano dati di validazione.
La categoria “metodi non normalizzati” comprende anche i metodi pubblicati dai produttori di materiali e kit, fatti validare a spese del produttore presso organismi che prestano questo servizio (ad esempio AFNOR Validation, Microval, Nordval). Appare chiaro che la validazione è presente ed è proprio quella reperibile sui siti ai link sopra, per i diversi metodi rientranti in questa categoria.
C’è anche un’ulteriore eccezione, che dovrebbe riguardare proprio alcuni metodi ISS…
Infatti al punto 7.2.2.1 si riporta che “I metodi validati da Laboratori/Centri di Riferimento Nazionali o Comunitari accreditati o da Centri di Referenza Nazionali accreditati e riconosciuti dall’Autorità centrale, possono essere utilizzati da altri Laboratori senza ulteriore validazione”.
Nello specifico dovrebbe trattarsi ad esempio di alcuni metodi ISS accreditati dai laboratori dell’Istituto come metodi interni e pubblicati nelle raccolte, riguardanti C. botulinum, allergeni, OGM, E. coli patogeni, Istamina, alcuni fitofarmaci, dettagli qui e qui. Sempre che l’Istituto vi fornisca la dichiarazione di validazione aggiornata.
Metodi sviluppati dal laboratorio
E i metodi sviluppati dal laboratorio? Anche secondo la lingua italiana sono quelli, per l’appunto, sviluppati dal laboratorio. Non sono “metodi sviluppati dal laboratorio” quelli modificati, adattati, ecc. Per questi si parla di “scostamento dai metodi”, nella ISO 17025 (punto 7.2.1.7, metodi per i quali al punto 7.2.2.1 si richiede la validazione).
Sì, certo, ma i famosi “metodi ufficiali”..? alla fine cosa sono?
Metodi “ufficiali”
Come dicevamo, non c’è una risposta univoca, vediamone alcune.
Cominciamo dalle più remote indicazioni della legge italiana, secondo la quale i “metodi ufficiali” (almeno per quanto riguarda gli alimenti) sono (erano, l’articolo è abrogato, secondo normattiva) quelli individuati dal Regio Decreto-Legge “Repressione frodi” n. 2033 del 15 ottobre 1925, all’art. 43: “Tutte le analisi occorrenti in applicazione del presente decreto saranno eseguite con i metodi ufficiali prescritti e i relativi certificati saranno rilasciati in esenzione dalla tassa di bollo”. Una serie di decreti ministeriali, emessi nel corso degli anni, ha reso disponibile una serie di raccolte di metodi ufficiali nell’ambito delle produzioni agricole, per suoli agricoli, sementi, fertilizzanti, vini, latte, formaggi, cereali. Da notare che tutti questi decreti fanno riferimento al regio decreto-legge originale.

Anche l’art. 21 della Legge 283/62 riportava (risulta abrogato dal D.Lgs. 27/2021, secondo normattiva) indicazioni sui “metodi ufficiali”, attribuendo la responsabilità per la loro definizione al Ministero della Sanità. Non risulta però siano mai stati pubblicati metodi secondo questa indicazione.
In ambito europeo non si parla di “metodi ufficiali di analisi” bensì di “metodi da utilizzare per il controllo ufficiale” o di “metodi di riferimento”. Ad esempio l’art. 5 del reg. CE 2073 del 2005 recita “I metodi di analisi e i piani e metodi di campionamento di cui all’allegato I sono applicati come metodi di riferimento”. Nell’allegato I sono indicati i principali metodi EN/ISO per le determinazioni microbiologiche, metodi che a questo punto assumono rilevanza “ufficiale”. Lo stesso avviene in altri casi per altri settori e matrici (ad esempio per il vino l’art. 120 octies del Reg. CE 1234 del 2007 individua i metodi OIV come metodi di analisi da utilizzare, seppur non riportando espressamente la locuzione “metodi ufficiali”. In questi casi il metodo pubblicato diventa “ufficiale” in quanto espressamente richiamato dalla legge. Non per gli arzigogoli dell’RT 08.
Esistono rari casi in cui il la norma cogente rimanda a qualche pubblicazione: anche in questo caso il metodo della pubblicazione diventa a tutti gli effetti “ufficiale”. Secondo RT 08 in questo caso non è richiesta alcuna validazione… o no? Vediamo meglio sotto, dove parliamo di “Verifica o validazione a cura del laboratorio”.
E poi esistono metodi autodefiniti “ufficiali”, come gli AOAC “Official methods”. Metodi che, per fortuna, sono validati.
Situazioni “ibride”, alquanto confuse e confondenti, si ritrovano in certi settori, come quello delle acque per consumo umano. Attualmente (speriamo che il prossimo recepimento della nuova direttiva europea sulle acque aggiusti la situazione, ma non ne siamo tanto sicuri, a giudicare dagli esordi), con le modifiche apportate dal D.M. 14 giugno 1017 al D.Lgs. 31/2001, si prevede l’accreditamento dei laboratori dei gestori di acquedotto o del controllo ufficiale entro il 31 dicembre 2019. La legge nulla prevede oltre a questo, riguardo ai metodi di analisi. Eppure è stato detto e ripetuto in numerosi convegni ed è convinzione diffusa tra gli addetti ai lavori che, nel “periodo transitorio” (non ancora di fatto terminato, visto che molti dei laboratori non sono accreditati per tutti i metodi o non lo sono del tutto), si sarebbero dovute seguire le indicazioni del Rapporto IstiSan 19/7 (che, ricordiamolo, non ha certo forza di legge), incluse quelle sulla scelta dei metodi analitici da seguire, ovvero di alcuni metodi da raccolta IstiSan. Poco chiaro? Ve lo avevamo detto che c’era confusione. In ogni caso i metodi IstiSan non sono “metodi ufficiali”.
Per orientarsi (a disposizione di tutti, anche di chi volesse redigere la prossima edizione del documento RT 08) ecco uno schema che illustra la situazione, con indicati su sfondo giallo i casi che, secondo la norma, richiedono validazione:
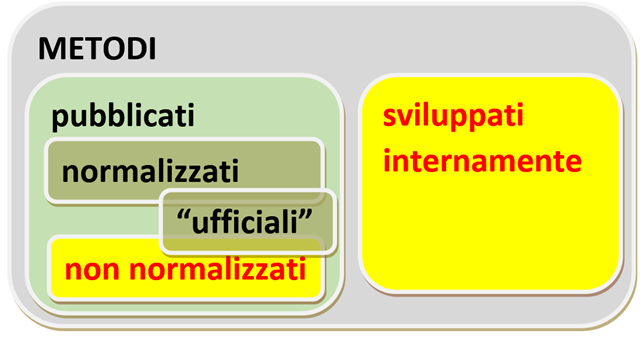
Metodi aggiornati e validi
La norma ISO 17025 ai punti 7.2.1.2 e 7.2.1.3 prescrive, semplicemente, l’utilizzo dell’ultima edizione valida dei metodi (“salvo che ciò non sia appropriato o possibile”), l’integrazione “con dettagli supplementari per assicurare una regolare e coerente applicazione” (le cosiddette “procedure di prova”), l’utilizzo di metodi appropriati scelti dal laboratorio “quando il cliente non specifica il metodo”, la preferenza per “metodi pubblicati in norme internazionali, regionali o nazionali o da organizzazioni tecniche autorevoli, o in testi o riviste di rilevanza scientifica, o indicati dal costruttore delle apparecchiature”, e indica la possibilità di utilizzare anche metodi sviluppati internamente, oppure modificati dal laboratorio.
Notiamo la traduzione infelice, una delle tante, di “regional” con “regionali”. No, non si tratta della celebre RMM (“Raccolta metodi molisani” che, a differenza della regione, non esiste), bensì, nel nostro caso italico, dei metodi europei, quelli pubblicati da CEN e CENELEC (siglati EN o CEN).
Verifica nel tempo?
La norma ISO 17025 prescrive al punto 7.2.1.5 di “verificare di essere in grado di eseguire correttamente i metodi prima di metterli in opera, assicurando di poter conseguire le prestazioni richieste”, di conservare le registrazioni della verifica, di ripetere la verifica “se il metodo viene revisionato dall’organismo che lo ha pubblicato”.
Da notare che nella norma non vi è alcuna richiesta di effettuare una verifica “nel tempo” del mantenimento delle prestazioni, un’attività che giustamente la norma prevede invece nell’ambito dell’assicurazione della validità dei risultati (punto 7.7) e che include “utilizzo di materiali di riferimento” e di “campioni di lavoro o di verifica”, “ripetizioni” (avrà forse a che fare con la ripetibilità?), “confronti interlaboratorio”. Per “monitorare le prestazioni” la norma indica anche il modo preferenziale: il confronto con altri laboratori.
Eppure nel documento RT 08 viene richiesto – abusivamente, l’ente di accreditamento NON è un ente normatore – di “verificare di mantenere nel tempo le prestazioni richieste”.
Già, per loro il punto 7.7 è “e adesso vediamo i circuiti interlaboratorio”…
Il laboratorio, secondo la ISO 17025, deve semplicemente garantire le prestazioni nel tempo, con riferimento ai risultati, non ripetere l’attività di verifica prestazionale iniziale, eppure molti ispettori ci assillano continuamente con richieste del tipo “ma quando scade la verifica?”. Come se fosse uno yogurt.

Verifica o validazione a cura del laboratorio per metodi “ufficiali”?!
Il documento RT 08 prescrive ai laboratori, per metodi normalizzati o metodi ufficiali (ma lo fa al punto 7.2.2.1, laddove l’argomento è “validazione”, altra confusione) di “determinare le caratteristiche prestazionali, qualora non riportate”, nonché di “verificare che le suddette prestazioni siano adeguate a soddisfare i requisiti cogenti e/o del cliente”.
Si tratta di una ripetizione di quanto già indicato al punto 7.2.1.5 “Qualora le caratteristiche prestazionali dei metodi non siano state definite, il Laboratorio deve determinarle”.
Questo è palesemente assurdo e vessatorio per quanto riguarda metodi normalizzati e “ufficiali”.
Riassumiamo, così è facile per tutti:
- Esiste un metodo “ufficiale” e normalizzato, ad esempio il metodo ISO 4833-1, il cui utilizzo è d’obbligo secondo reg. CE 2073 del 2005
- L’ente emittente (esempio ISO) non si è preoccupato di effettuare una validazione ma ha raccattato dati parziali qua e là, e pubblica solo il riferimento valido per latte crudo o pastorizzato (in bibliografia, peraltro, e con riferimento a pubblicazioni vecchie di trent’anni e più)
- È obbligatorio usare quel metodo per una determinata finalità (controllo degli alimenti, non solo del latte crudo o pastorizzato)
- È il laboratorio a dover determinare le caratteristiche prestazionali, di fatto a eseguire le attività tipiche della validazione del metodo!
- È il laboratorio a dover verificare che le prestazioni soddisfino i requisiti cogenti, quando il metodo è quello obbligatorio per legge!
Ricordiamo che invece la norma ISO 17025 richiede validazione solo per i metodi non normalizzati e per quelli sviluppati dal laboratorio. Non per quelli normalizzati! E ricordiamo che “normalizzato” non vuol dire necessariamente “validato”. Molti metodi normalizzati non riportano dati di validazione.
Verifica o validazione a cura del laboratorio per metodi validati?!
Sempre nel punto sbagliato (7.2.2.1) del documento RT 08 si afferma che “Nel caso in cui il metodo non normalizzato sia stato validato da una organizzazione terza indipendente o da organismi di certificazione di prodotto accreditati (es. AFNOR), il Laboratorio deve verificare di rientrare nei valori dei parametri prestazionali della validazione”. Siamo sempre nel paragrafo che riguarda i metodi non normalizzati.
Ma questa è una verifica prestazionale!
In sostanza una inutile ripetizione di quanto già detto al punto 7.2.1.5 della ISO 17025, ripetizione foriera di ulteriore confusione.
Metodi “interni”, correttamente “sviluppati dal laboratorio”
Di “metodi sviluppati dal laboratorio” si tratta al punto 7.2.1.6 della norma, laddove sono definite le regole e le responsabilità per lo sviluppo. Si tratta a tutti gli effetti di un processo di progettazione.
Non è affatto corretto, come invece si fa nel documento RT 08, affermare che “Le edizioni non più in vigore di norme o metodi di prova ufficiali, insieme con i progetti di norma non ancora nella forma sottoposta al voto finale, sono classificati tra i devono essere trasformati in metodi di prova sviluppati dal Laboratorio”.
Lasciamo stare il fatto che nemmeno con l’errata corrige, al terzo tentativo, non siano riusciti a sistemare la frase (“sono classificati tra i devono essere trasformati in metodi di prova”), e passiamo ai fatti: in questo caso il laboratorio non sviluppa alcunché. È un fatto.
Semplicemente, l’abrogazione della norma cogente o il ritiro della norma volontaria fanno sì che il metodo da “normalizzato” diventi semplicemente “pubblicato”, “non normalizzato”, quindi richieda la validazione.
E come fare la validazione in questi casi? Non ci sembra ad esempio un’idea peregrina farla su base “storica”: il metodo ha funzionato egregiamente fino ad oggi, perché mai non dovrebbe più funzionare? Sì, forse potrebbe dare dei risultati diversi dalla nuova edizione aggiornata, e allora la validazione sarà semplicemente il confronto delle prestazioni tra le due versioni. E, se il cliente richiede proprio il metodo superato, è evidente che questo “soddisfa le esigenze per l’applicazione”. Quindi è valido.
Curioso che però, in questo caso, il laboratorio debba comunque inserire in accreditamento anche il metodo aggiornato, che magari non utilizza mai. Misteri accredini. A che pro?
Ci sembra invece corretto considerare come “sviluppo”, come si afferma in RT 08, i casi in cui:
- Si cambia tecnica analitica;
- Si eliminano fasi (ma per quanto riguarda le conferme?);
- Si usano dotazioni (apparecchiature, materiali, ecc.) con prestazioni (caratteristiche) inferiori a quelle previste.
In questi casi, a tutti gli effetti, il laboratorio “progetta” modifiche, e quelle modifiche dovrà validare.
L’RT 08 concede un’eccezione per i metodi non più in vigore richiamati da disposizioni cogenti o capitolati:
“Fanno eccezione le edizioni superate di norme ed i progetti di norma quando sono richiamati da disposizioni cogenti, da capitolati della Pubblica Amministrazione, o da norme per la certificazione di prodotto, in vigore, o richiesti da organismi notificati”
In questo caso però non è chiaro se sia richiesta o meno la validazione. La frase che precede è riferita solo alla “trasformazione in metodo sviluppato dal laboratorio”.
Figli e figliastri
Ci sono poi delle situazioni alquanto curiose, strane, e non vogliamo andare oltre con gli aggettivi.

Parliamo ad esempio dei metodi CCFRA. In particolare la raccolta CCFRA G 43 del 2003/2007.
Qualcuno li conosce? Noi sì: ai tempi del SINAL ponemmo la questione sotto forma di non conformità a un laboratorio, ora non più attivo in quel settore, in quanto i suddetti metodi, essendo emessi da una società privata (Campden BRI, che offre servizi analitici e di consulenza), non potevano essere considerati normalizzati, bensì “pubblicati” (e nemmeno tanto, in quanto all’epoca non accessibili), quindi necessitanti di validazione. Il laboratorio era l’unico in Italia ad utilizzarli e non li aveva affatto validati. Alcuni bandi richiedevano proprio di utilizzare quei metodi. Strano no? Come andò a finire? La non conformità venne annullata. Ancora più strano, no?
Diversi lustri dopo qual è la situazione?
La raccolta non risulta più presente sul sito Campden BRI, quindi sembrerebbe non più in vigore. Sette laboratori risultano però ad oggi accreditati per uno o più metodi della raccolta. Non ci è dato a sapere se hanno provveduto a validazione.
Che fare?
Abbiamo cercato di dare qualche orientamento e suggerimento nel testo. Intanto cerchiamo con questo di avere idee chiare almeno noi. Speriamo poi che il prossimo RT 08 sia scritto in maniera meno caotica, non solo al punto 7.2.
Per cercare di chiarire ulteriormente, per l’ambito microbiologico, si può approfondire qui l’argomento.
Buon lavoro!
4 novembre 2022
Commenti recenti